아무래도 연초라 이래저래 회사일로 바쁘고 이제 곧 석사학위 논문 작성을 해야 되는 터라 합격은 기대도 안하고 이렇게 논문방향과 일치하는 부분만 작성해서 올려야 할 것 같습니다.
첫번째로 분석화학과 전기화학에 대해서 조금 알아보려고 합니다.
분석화학이란 미지의 물질 또는 시료에 대해 정성 또는 정량 분석을 하는 데 목적을 두고 있습니다.
즉, 특정 혼합물에, 특정 물질 혹은 특정 공간에 어떠한 물질이 얼마나 포함되어 있는가를 알아내는 방법론에 대한 과목을 다루고 있는 게 분석화학입니다.
분석법의 종류로는
1) 무게 분석법 - 침전 외
2) 부피 분석법 - 적정 외
3) 기기 분석법 - 분광화학분석 / 전기화학분석 / 분리분석 외
가 있습니다. 그 중에서도 저는 이차전지 양극재가 테마이기 때문에 전기화학분석이 가장 도움이 되는 것 같습니다.
(물론 원료 재활용 공정 중에서는 분광화학분석 등을 사용하긴 합니다.)
전기화학은 말 그 대로 전기와 화학을 이용하는 것입니다. 보통 산화-환원 반응(Redox Reaction)을 이용하여 전자의 주고 받음을 이용해서 물질을 정성 또는 정량 분석을 합니다.
전기화학 분석 방법에는 산화-환원 적정법 / 전하량법 / 전위전류법 / 전위차법 / 전자무게분석법이 있습니다.
전기화학은 산화-환원 반응 즉, 전자의 이동입니다.

간단하게 설명하자면 두 개의 금속 막대는 전극입니다. 건전지처럼 (+)와 (-)극이 존재하여 두 극간의 전위차가 발생하여 한 쪽 방향으로 전자가 이동하게 되고 전위차가 같아질 때, 방전이 이루어지게 됩니다.
여기서 산화가 일어나는 전극을 산화전극(Anode) 이라고 하며, 환원이 일어나는 전극을 환원 전극(Cathode)이라고 합니다. 전기화학에서 관례상으로 왼쪽을 산화전극(Cu), 오른쪽을 환원전극(Ag) 으로 둡니다.
기존의 반도체에서 Cathode는 음극, Anode는 양극으로 알고 계신 분들은 여기서 개념을 다시 잡으셔야합니다. 산화, 환원으로 기억을 하시는 편이 더 유용합니다.
비커는 전해액을 담고 있는 역할이고 용액은 전해액 입니다.
이 전해액이 분석하고자 하는 분석의 대상이 됩니다. 똑같은 농도에 똑같은 화합물이 아닌 이상 한쪽은 산화로 인해 전자를 잃고 한쪽은 환원으로 인해 전자를 얻게 됩니다.
금속의 이온화 경향을 본다면 칼슘<칼륨<나트륨<마그네슘<알루미늄<아연<철<니켈<주석<납<수소<구리<수은<은<백금<금 순서로 전자를 얻는 환원 성질의 경향성을 띕니다.
전위는 절대적으로 측정할 수 없기 때문에 항상 전위차를 논합니다. 그러기에 수소는 표준수소전극 : SHE (Standard hydrogen electrode)로 사용되어 수소 전위 값을 0 V로 두고 나머지 금속과의 전위차를 논할 때 사용됩니다.
그림에서 Ag+ 와 Cu+가 있습니다. 경향성에 의하면 Ag+ + e- -> Ag(s)가 되고 Cu -> Cu 2+ + 2e-가 되므로 Ag+의 양은 전자를 받으면서 감소하게 되고 Ag 막대의 질량은 증가하게 될 것입니다. 반대로, Cu 막대의 양은 줄어들고 Cu2+의 양은 늘어나게 되겠죠
마지막으로, 염다리 (유리 다리)는 실험의 오차를 줄이기 위해 설치해 놓은 장치입니다.
Ag+와 Cu2+의 경향성으로 보면 왼쪽의 산화전극에서는 Cu2+의 양이 늘어 양전하가 늘어나고 반대편은 Ag+의 양이 줄어 반응에 참여하지 않은 NO3- 만 남아 음전하를 띄게 될 것입니다.
그렇게 되면 화학종의 전위차에 의해 분석을 해야하는데 단순 전하량의 차이로 제대로 된 측정을 할 수 없게 됩니다. 즉, 분석을 할 때 측정마다 동일한 환경이 아니게 됩니다. 그래서 염다리를 설치해 주는 것이 염다리 속은 KCl의 겔 형태로 일종의 막 역할을 하여 분석 물질들과 혼합하지 못하게 하여 양전하가 늘어나는 곳에는 Cl-가 이동하고 음전하가 늘어나는 곳에는 K+가 이동하여 전하의 불균형을 해결해줍니다.
이러한 전지의 그림을 표현하는 식은
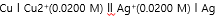
구리전극 / 구리이온의 농도 // 은이온의 농도 / 은전극 으로 표시하게 됩니다.
(염다리)
이 표현식은 전위차법 등 분석법에 있어서 전극 표시를 해줄 때 필수적으로 해주기 때문에 매우 중요합니다.
이는 전기화학의 기본 토대가 되기 때문에 이해를 하셔서 하시는 연구 및 공부에 도움이 되었으면 좋겠습니다.
감사합니다!
'자격증' 카테고리의 다른 글
| [화학분석기사] 제벡 효과, 펠티에 효과, 톰슨 효과 (2) | 2023.02.09 |
|---|---|
| [화학분석기사] 시험 검사 결과의 기록 방법 (0) | 2023.02.07 |
| [화학분석기사] 스타트 (0) | 2023.01.20 |
| 현재 보유 자격증 (0) | 2023.01.09 |
